A utilização do trióxido de arsênico no tratamento da leucemia promielocítica aguda (LPA)
Veja a seguir estudos clínicos sobre a utilização do trióxido de arsênico em pacientes com LPA, seus benefícios e recomendações atuais
Em 1957, Hillestad descreveu três pacientes com leucemia aguda rapidamente fatal, com coagulopatia severa e um número abundante de promielócitos anormais.1 Foi a primeira descrição de uma leucemia promielocítica aguda (LPA), uma leucemia mieloide aguda (LMA) em que uma translocação entre os cromossomos 15 e 17 – t(15;17)(q22;q12) – forma um gene de fusão, PML-RARA, que sintetiza uma proteína que causa um bloqueio de maturação e aumento na proliferação de promielócitos patológicos.2-4

Diagnóstico e casos clínicos da LPA
O diagnóstico é feito a partir da confirmação da presença do PML-RARA por técnicas moleculares.5
O quadro clínico típico de uma LPA inicial está associado a coagulopatia de consumo, assim como hiperfibrinólise, sendo que hemorragias cerebrais e pulmonares são as causas mais comuns de óbito antes do início do tratamento. Desse modo, a LPA é considerada uma emergência médica, estando indicado início de ácido all-trans retinóico (ATRA) à suspeita dessa patologia, mesmo antes da confirmação diagnóstica.5
Medidas de tratamento e consequências do processo protocolar
Outras medidas iniciais extremamente importantes são:
- suporte transfusional para controle dos distúrbios de coagulação (transfusão de plaquetas, fibrinogênio e/ou crioprecipitado, plasma fresco congelado);
- controle de leucocitose (citorredução caso haja mais de 10 mil leucócitos ao diagnóstico);
- controle de síndrome de diferenciação.5
Essas meddas iniciais foram responsáveis por uma redução expressiva da mortalidade inicial. Em relação ao tratamento específico da LPA, o uso de ATRA associado a quimioterapia tornou a LPA uma neoplasia altamente curável, com vários estudos mostrando sua eficácia, inclusive tornando-se a terapia padrão até alguns anos atrás.6
Apesar das altas taxas de curas, esses protocolos estão frequentemente associados com toxicidade hematológica grave e desenvolvimento de neoplasias secundárias em aproximadamente 2% de pacientes.7
Tratamento de LPA com trióxido de arsênico
O trióxido de arsênico (ATO) é considerado uma das medicações mais eficazes no tratamento da LPA. Estudos preliminares conduzidos na China e nos Estados Unidos demonstraram que seu uso como agente único levou a remissão molecular sustentada em pacientes com recaída após tratamento com protocolos baseados em ATRA.8-11
O ATO se liga à porção PML da proteína PML-RARA, levando à sua degradação; consequentemente, há retorno da hematopoese normal, já que o bloqueio de diferenciação ocasionado pelo PML-RARA não está mais presente. O ATRA age de maneira sinérgica ao ATO, porque se liga à porção RARA da proteína, também levando à sua degradação. Esse efeito sinérgico foi demonstrado tanto em testes in vitro quanto em testes clínicos, mantendo a alta eficácia do tratamento com muito menos toxicidade.12-16
A partir desses fatos, na última década foram publicados vários estudos fase 3 que solidificaram o papel do ATO na primeira linha do tratamento da LPA.
Estudos clínicos sobre a utilização de ATO + ATRA no tratamento da LPA
Estudos fase 3 do grupo italiano GIMENA
Em 2013, o New England Journal of Medicine publicou um estudo fase 3 liderado pelo grupo italiano do GIMEMA, de não inferioridade, com desfecho primário de sobrevida livre de eventos (EFS – event free survival) em dois anos, comparando em primeira linha o tratamento padrão ATRA + quimioterapia contra ATO + ATRA, em pacientes adultos com LPA de risco baixo ou intermediário (abaixo de 10 mil leucócitos ao diagnóstico).17
Como demonstrado na Figura 1, o tratamento com ATO + ATRA requer um tempo muito menor de tratamento, já que não requer manutenção por dois anos após os ciclos de consolidação.17
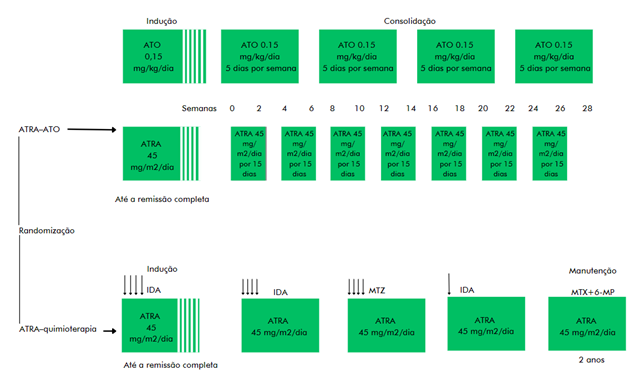
Um desfecho secundário muito relevante é a toxicidade hematológica, muito menor no braço sem quimioterapia17 (Figura 2).
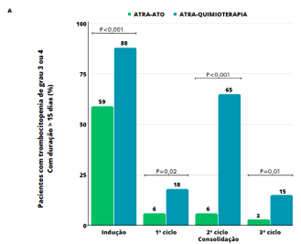
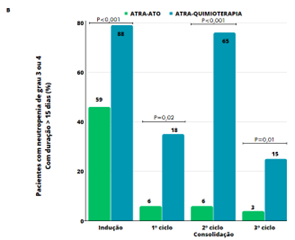
ATO: trióxido de arsênico; ATRA: ácido all-trans retinóico.
Adaptada de: Lo-Coco Fe, et al., 2013.17
Estudo fase 3 AML17
Estudo fase 3 APL0406
Em 2017, foi publicada a análise final do estudo fase 3 APL040619. Nesse estudo, 263 pacientes com LPA de risco baixo ou intermediário (< 10 mil leucócitos) foram randomizados para ATO + ATRA ou ATRA + quimioterapia.
Com um follow-up mais longo, de 40,6 meses, o estudo demonstrou uma diferença estatisticamente significativa de benefícios para o braço ATO + ATRA em relação à sobrevida livre de eventos, sobrevida livre de doença, incidência cumulativa de recaída e uma tendência de aumento de sobrevida global.19
Os dois maiores efeitos no grupo chemo-free foram aumento de transaminases (na maioria das vezes transitório) e aumento do intervalo QTc (também facilmente manejável, sem nenhum óbito associado com os devidos cuidados).19
European LeukemiaNet
Considerando esses robustos dados, não surpreende que em 2019 tenham sido publicadas as orientações do European LeukemiaNet,5 recomendando a associação de ATO + ATRA em primeira linha em pacientes com LPA não alto risco.
Nos pacientes com LPA de alto risco, também é possível utilizar ATO + ATRA com algum quimioterápico associado (geralmente em doses menores), para controle de leucocitose e evitar síndrome de diferenciação, além disso, se recomenda ATO + ATRA em pacientes em recaída após tratamento com ATRA + quimioterapia.5
As recomendações incluem os cuidados ao utilizar o ATO5 (Tabela 1).
Tabela 1. Recomendações de ATO
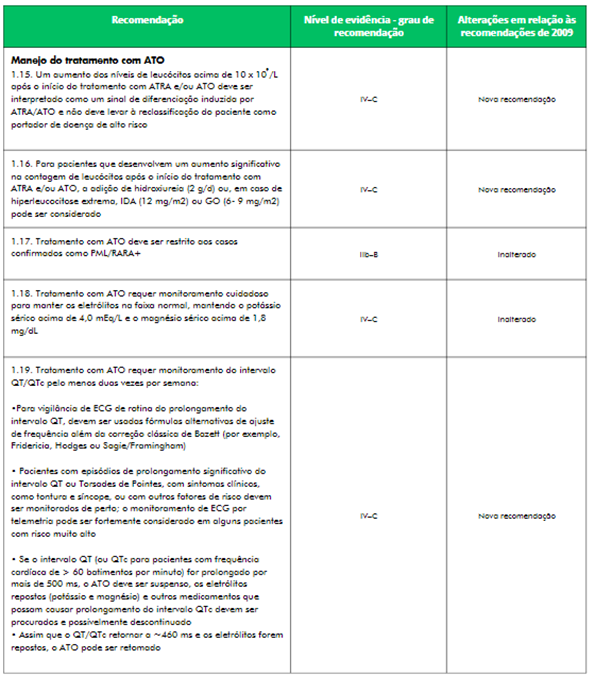
Conclusão da revisão sobre o uso de ATO + ATRA no tratamento da LPA
ATO é uma medicação extremamente eficaz na LPA, segura, com alto potencial de cura quando associado ao uso de ATRA, com perfil de toxicidade muito melhor quando comparado com a quimioterapia convencional.
Referências
- Hillestad LK. Acute promyelocytic leukemia. Acta Med Scand. 1957;159:189-94.
- WHO Classification of Tumours of Haematopoietic and Lymphoid Tissues. 4th ed.; 2008.
- Wang ZY, Chen Z. Acute promyelocytic leukemia: from highly fatal to highly curable. Blood 2008;111(5):2505-15.
- Zhou J, Pérès L, Honoré N, Nasr R, Zhu J, de Thé H. Dimerization-induced corepressor binding and relaxed DNA-binding specificity are critical for PML/RARA-induced immortalization. Proc. Natl Acad. Sci. USA. 2006;103:9238-43.
- Sanz MA, Fenaux P, Tallman MS, Estey EH, Löwenberg B, Naoe T, et al. Management of acute promyelocytic leukemia: updated recommendations from an expert panel of the European LeukemiaNet. Blood 2019;133(15):1630-43.
- Sanz MA, Grimwade D, Tallman MS, Lowenberg B, Fenaux P, Estey EH, et al. Management of acute promyelocytic leukemia: recommendations from an expert panel on behalf of the European LeukemiaNet. Blood 2009;113:1875-91.
- Montesinos P, González JD, González J, Rayón C, de Lisa E, Amigo ML, et al. Therapy-related myeloid neoplasms in patients with acute promyelocytic leukemia treated with all-trans-retinoic acid and anthracycline-based chemotherapy. J Clin Oncol. 2010;28(24):3872-9.
- Zhang P, Wang SY, Hu LH. Arsenic trioxide treated 72 cases of acute promyelocytic leukemia. Chin J Hematol. 1996;17:58-62.
- Shen ZX, Chen GQ, Ni JH, Li XS, Xiong SM, Qiu QY, et al. Use of arsenic trioxide (As2O3) in the treatment of acute promyelocytic leukemia (APL): II. Clinical efficacy and pharmacokinetics in relapsed patients. Blood 1997;89(9):3354-60.
- Soignet SL, Frankel SR, Douer D, Tallman MS, Kantarjian H, Calleja E, et al. United States multicenter study of arsenic trioxide in relapsed acute promyelocytic leukemia. J Clin Oncol. 2001;19(18):3852-60.
- Breccia M, Lo-Coco F. Arsenic trioxide for management of acute promyelocytic leukemia: current evidence on its role in frontline therapy and recurrent disease. Expert Opin Pharmacother. 2012;13:1031-43.
- Shao W, Fanelli M, Ferrara FF, Riccioni R, Rosenauer A, Davison K, et al. Arsenic trioxide as an inducer of apoptosis and loss of PML/RAR alpha protein in acute promyelocytic leukemia cells. J Natl Cancer Inst. 1998;90(2):124-33.
- Zhu J, Koken MHM, Quignon F, Chelbi-Alix MK, Degos L, Wang ZY, et al. Arsenic-induced PML targeting onto nuclear bodies: implications for the treatment of acute promyelocytic leukemia. Proc Natl Acad Sci U S A 1997;94(8):3978-83.
- Lallemand-Breitenbach V, Guillemin MC, Janin A, Daniel MT, Degos L, Kogan SC, et al. Retinoic acid and arsenic synergize to eradicate leukemic cells in a mouse model of acute promyelocytic leukemia. J Exp Med. 1999;189(7):1043-52.
- de Thé H, Chen Z. Acute promyelocytic leukemia: novel insights into the mechanism of cure. Nat Rev Cancer 2010;10:775-83.
- Hu J, Liu YF, Wu CF, Xu F, Shen Z-X, Zhu Y-M, et al. Long-term efficacy and safety of all-trans retinoic acid/arsenic trioxide-based therapy in newly diagnosed acute promyelocytic leukemia. Proc Natl Acad Sci U S A 2009;106(9):3342-7.
- Lo-Coco F, Avvisati G, Vignetti M, Thiede C, Orlando SM, Iacobelli S, et al. Retinoic acid and arsenic trioxide for acute promyelocytic leukemia. N Engl J Med. 2013;369(2):111-21.
- Burnett AK, Russell NH, Hills RK, Bowen D, Kell J, Knapper S, et al. Arsenic trioxide and all-trans retinoic acid treatment for acute promyelocytic leukaemia in all risk groups (AML17): results of a randomised, controlled, phase 3 trial. Lancet Oncol. 2015;16(13):1295-305.
- Platzbecker U, Avvisati G, Cicconi L, Thiede C, Paoloni F, Vignetti M, et al. Improved Outcomes With Retinoic Acid and Arsenic Trioxide Compared With Retinoic Acid and Chemotherapy in Non-High-Risk Acute Promyelocytic Leukemia: Final Results of the Randomized Italian-German APL0406 Trial. J Clin Oncol. 2017;35(6):605-12.